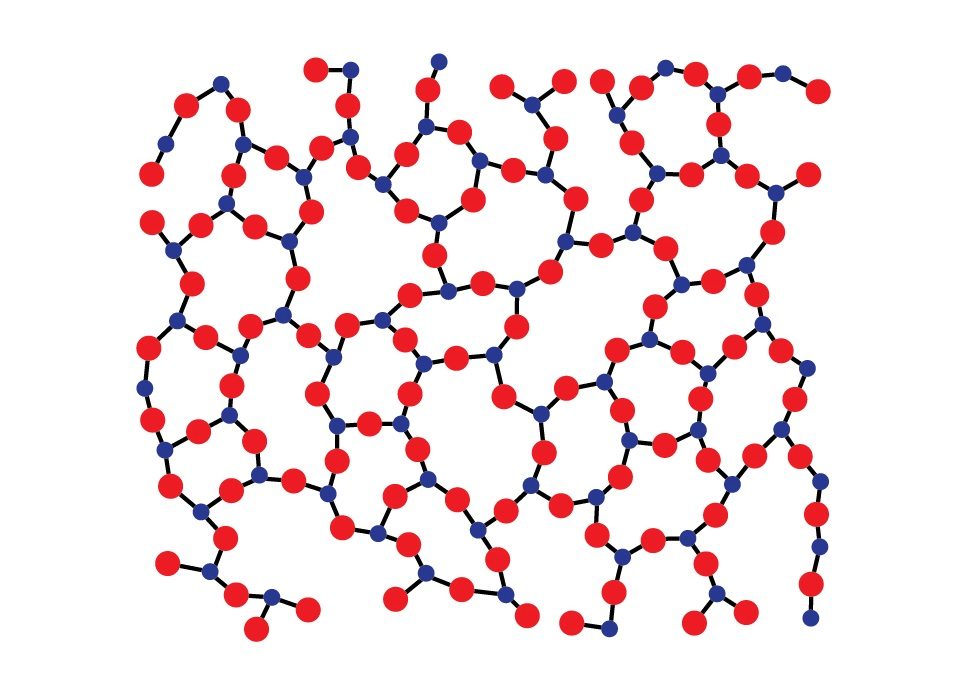
Les solides sont divisés en corps amorphes et cristallins, en fonction de leur structure moléculaire et de leurs propriétés physiques.
Contrairement aux cristaux, les molécules et les atomes des solides amorphes ne forment pas un réseau, et la distance entre eux fluctue dans un certain intervalle de distances possibles. En d’autres termes, dans les cristaux, les atomes ou les molécules sont mutuellement disposés de telle sorte que la structure formée peut être répétée dans tout le volume du corps, ce que l’on appelle l’ordre à longue portée. Dans le cas des corps amorphes, la structure des molécules n’est préservée que par rapport à chaque molécule, il y a une régularité dans la distribution des molécules voisines — l’ordre proche. Un exemple clair est présenté ci-dessous.
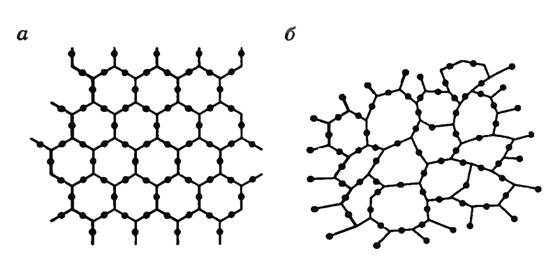
La figure de gauche (a) montre le réseau de molécules de quartz, et celle de droite (b) l’arrangement des molécules de verre de quartz, qui est un corps amorphe.
Les corps amorphes comprennent le verre et d’autres substances à l’état vitreux, la colophane, les résines, l’ambre, la cire d’étanchéité, le bitume, la cire, ainsi que des substances organiques : caoutchouc, cuir, cellulose, polyéthylène et autres.
Table des matières
Propriétés des corps amorphes
La particularité de la structure des solides amorphes leur confère des propriétés individuelles :
- La fluidité faiblement prononcée est l’une des propriétés les plus connues de ces corps. La fluidité faiblement prononcée est l’une des propriétés les plus connues de ces corps. Un exemple serait l’écoulement du verre qui est resté longtemps dans le cadre d’une fenêtre.
- Les solides amorphes n’ont pas de point de fusion défini, car le passage à l’état liquide lors du chauffage se fait progressivement, par ramollissement du corps. C’est pour cette raison que l’on applique à ces solides ce que l’on appelle la plage de température de ramollissement.
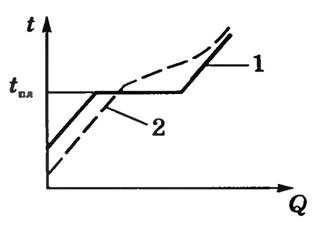
Le graphique de la transition d’un corps amorphe à l’état liquide est représenté par une ligne pointillée (2), tandis que le graphique de la transition d’un corps solide normal à l’état liquide est représenté par une ligne pleine (1).
- En raison de leur structure, ces corps sont isotropes, c’est-à-dire que leurs propriétés physiques ne dépendent pas du choix de la direction.
- Une substance à l’état amorphe a une énergie interne plus élevée qu’à l’état cristallin. C’est pourquoi les corps amorphes sont capables de passer d’eux-mêmes à l’état cristallin. Ce phénomène peut être observé en raison de l’opacification des verres au fil du temps.
L’état vitreux
Dans la nature, il existe des liquides qu’il est pratiquement impossible de transformer en état cristallin par refroidissement, car la complexité de leurs molécules ne leur permet pas de former un réseau cristallin régulier. Les molécules de certains polymères organiques font partie de ces liquides.
Matériaux par thème

Cependant, par un refroidissement profond et rapide, presque toutes les substances sont capables de passer à l’état vitreux. Il s’agit d’un état amorphe qui n’a pas de réseau cristallin évident, mais qui peut se cristalliser partiellement, à l’échelle de petits amas. Cet état de la matière est métastable, c’est-à-dire qu’il persiste dans certaines conditions thermodynamiques requises.
À l’aide d’une technologie de refroidissement à une certaine vitesse, la substance n’aura pas le temps de cristalliser et se transformera en verre. En d’autres termes, plus la vitesse de refroidissement du matériau est élevée, moins il est susceptible de cristalliser. Par exemple, le verre métallique nécessite une vitesse de refroidissement de 100 000 à 1 000 000 Kelvin par seconde.
Dans la nature, la substance existe à l’état vitreux et provient du magma volcanique liquide, qui se refroidit rapidement lorsqu’il entre en contact avec de l’eau froide ou de l’air. Dans ce cas, la substance est appelée verre volcanique. On peut également observer du verre formé par la fusion d’une météorite en interaction avec l’atmosphère — verre météoritique ou moldavite.

Moldavite, verre naturel formé par l’impact d’une météorite, à Besedin, en Bohême, République tchèque.
Date de publication: 12-26-2023
Mettre à jour la date: 12-26-2023
